先日重症筋無力症の新規薬剤ウィフガートの薬価が決まったことを確認しましたが、その際に一緒に薬価が決定されていたのが、片頭痛の新規急性期治療薬のラスミジタンlasmiditanです。商品名としては「レイボー」でイーライリリーが製造し、第一三共が販売する形のようです。薬価は100mgが570.9円、50mgが324.7円です。
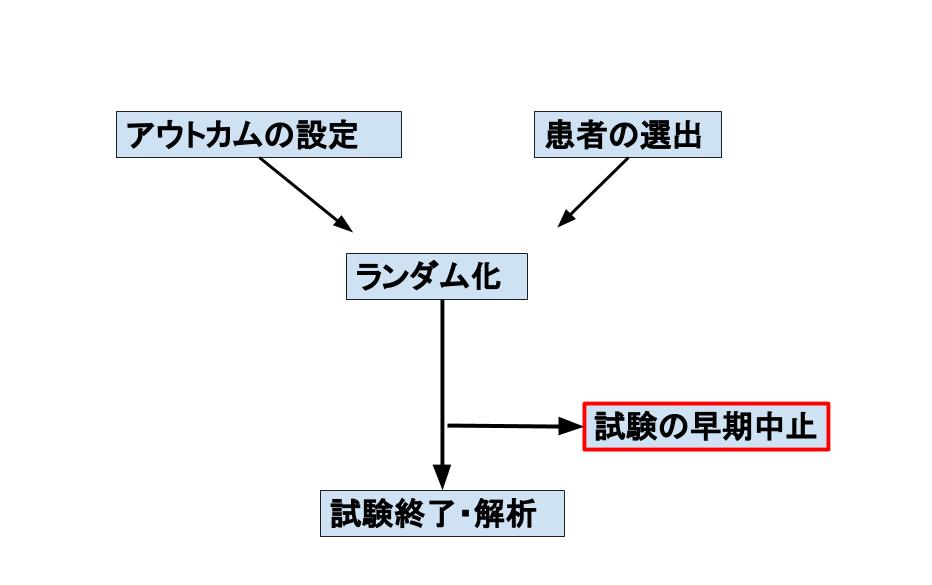
片頭痛は非常にコモンな疾患なので日常診療でもよく診ますし、なんなら自分も片頭痛があるので興味がありますが、急性期治療の第3相試験を読んだことはあまりなかった(トリプタン以来新規薬剤が日本で採用なかったのもありますが)ので、lasmiditanの第3相試験のうちの一つであるSPARTANを読んでみようと思います。
ちなみにもう一つの第3相試験はSAMURAIなんですが、この辺のネーミングセンスはなんなんですかね、、。SPARTANに至っては前立腺癌の試験とも名前被っちゃってるようです。
では、周辺知識もまとめながら紹介してみます。
片頭痛の急性期治療
片頭痛の急性期治療はNSAIDsなどの通常の鎮痛薬、トリプタン製剤が主体となっていました。
NSAIDsはエビデンスもあり、安価であるため、軽度の片頭痛であればそれだけで十分コントロールできます。トリプタン製剤もエビデンスがかなり蓄積されてきており、NSAIDsだけで不十分な場合は使用されます。値段は少し上がりますが、今は後発品も出てきていますね。さらに、その後メカニズムの解明に伴って新薬が徐々に登場してきます。
片頭痛の原因となる分子として注目されたのがcalcitonin gene-related peptide(CGRP)でした。トリプタン製剤は5-HT1B/1D受容体作用するアゴニストとしてCGRPの分泌を阻害し、片頭痛発作を抑える作用を持ちます。ただ血管収縮作用も持ってしまうため血管疾患の既往に対して禁忌となるのがデメリットでした。
これに対して今回主題となるlasmiditanなどの-ditan系と言われる薬剤は中枢や末梢の三叉神経細胞にある5-HT1F受容体に選択的に結合することからそういったデメリットがないことが期待されます。今まで日本でこの系統の薬剤は採用がありませんでした。
また同じくCGRPに着目したものとしてはCGRPの拮抗薬である-gepant系もありますが、こちらも日本では採用がありません。抗CGRPモノクローナル抗体であるアジョビ、エムガルティは昨年から採用となっています。ただ、これらは急性期治療薬ではなく、発作予防薬なので今回の話からは少し外れます。
なお、この辺りの全体の話は2020年のNEJMのnarrative reviewで簡潔にまとまっていますので気になる方はどうぞ。
Migraine | NEJM
SPARTAN(LAHK試験)の概要
それでは今回読んでいく論文はこちらです。
Phase 3 randomized, placebo-controlled, double-blind study of lasmiditan for acute treatment of migraine
lasmiditanの有効性を評価するための二重盲検ランダム化比較試験でプラセボと50mg, 100mg, 200mgを比較した試験となっています。
アメリカ、イギリス、ドイツの頭痛センター、125施設の患者を対象としており、2016年5月から2017年6月まで患者が募集されました。比較的短期間に見えますが、これで目標サンプルサイズが集まるので、片頭痛がいかに多い疾患かよくわかりますね。
同じ第3相試験でもSAMURAI(LAHJ試験)は50mgが含まれていません。日本では50mg錠も採用となっているため、この用量について効果や副作用を考えるにはこちらのstudyが参考になるでしょう。もう一つの試験であるSAMURAIの論文はこちらとなっています。
Lasmiditan is an effective acute treatment for migraine
また、SAMURAIと言いながらこちらも海外試験であり、国内試験は第2相試験であるMONONOFU(LAIH試験)のみとなっています。これまたネーミングがアレですが、、、。
Phase 2 randomized placebo‐controlled study of lasmiditan for the acute treatment of migraine in Japanese patients
PICOの整理
では試験の内容をPICOに則って整理してみます。
P:
・inclusion criteria
18歳以上、1年以上の病歴の片頭痛(前兆の有無は問わない)
MIDAS score 11点以上
発症が50歳未満
3-8回/月の頻度で発作がある
・exclusion criteria
慢性片頭痛やほかの一次性・二次性頭痛の病歴がある(薬剤誘発性頭痛など)
12か月以内に月15回以上の頭痛発作があるB
脳出血、てんかんなどけいれんのリスクが高い
めまいを繰り返している(BPPV,メニエール病など)
合併症のある糖尿病
起立性低血圧による失神がある
腎不全、肝不全
薬物依存がある
自殺リスクが高い
オピオイド、バルビツレート系薬剤や頭痛の頻度を低下させる薬を試験参加の3カ月以内に開始している
ここで確認しておきたいのはMIDAS scoreです。片頭痛の程度を表したスコアリングで、大まかに頭痛の頻度や程度を評価することができます。11点以上ということは中等度以上の患者層を含んでいるということになります。
片頭痛の程度を評価するためのスコアです。
3カ月以内に何日くらい仕事(あるいは家事)ができなかったか、あるいは何日くらい仕事量が半減したかを尋ねて足し合わせることで、点数付けして判断する簡便なもので、妥当性についてもすでに十分に検討されているようです。
QxMDのようなツールにも搭載されているようなので具体的な内容を見たい人はこちらをどうぞ。
MIDAS (Migraine Disability Assessment) | QxMD
MIDAS scoreが評価されている主要な論文はこちらです。
Validity of the Migraine Disability Assessment (MIDAS) score… : PAIN
また、もう一つ着目しておきたいのは、トリプタン製剤では血管収縮作用のため禁忌となる心筋梗塞などの血管疾患やコントロール不良の高血圧の患者も含みうる点です。
機序としてもトリプタン製剤と異なることからそうした疾患のある方への選択肢としては有用と考えられます。
I,C:
最長8週間の観察期間中に起きた頭痛に対して、ランダム割り付けされたプラセボ(コントロール群)もしくは実薬(介入群)を発作から4時間以内に内服。
最初の内服としてはlasmiditan 200mg,100mg,50mgとプラセボを
1:1:1:1割り付けしています。
また、初回内服の2-24時間以内で、頭痛が持続あるいは再燃した場合は2回目の内服も可とされています。
2回目の内服としては
lasmiditan or プラセボ
を2:1割り付けされています。
なお、患者・調査者・スポンサーのいずれも割付について盲検化されています。
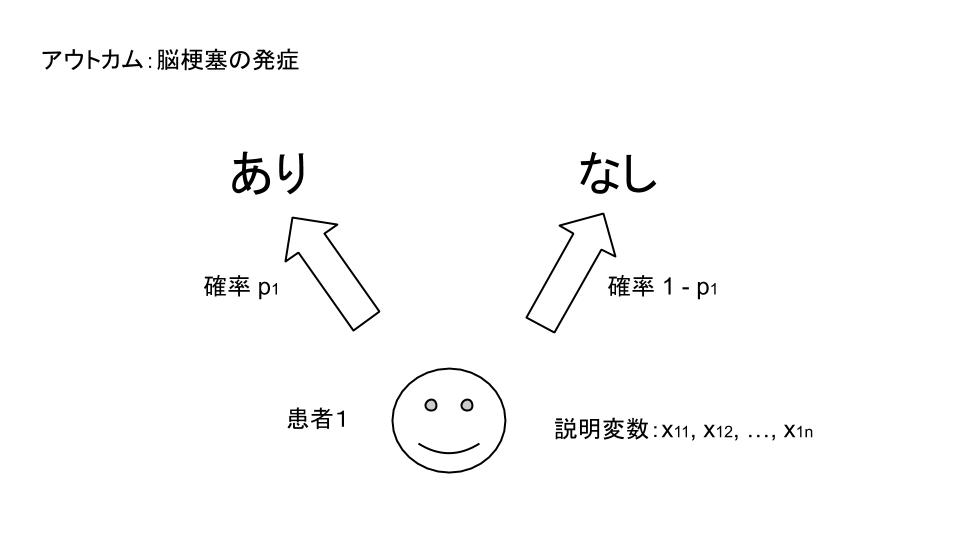
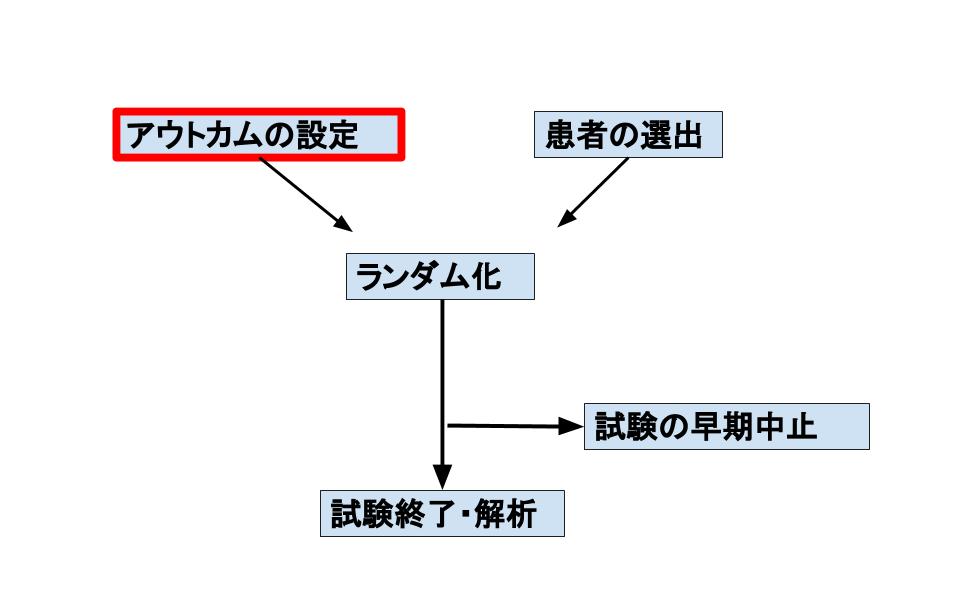
O:
アウトカムは
- 内服後2時間で頭痛がなくなった(pain-free)患者の割合
- most bothering symptoms(MBS)の改善が得られた患者の割合
の2つとしています。
pain-freeの判定は、電子日記を使って内服後0.5, 1, 1.5, 2, 3, 4, 24, 48時間後の頭痛の強さ(0~3点)を記録しており、2点(moderate), 3点(severe)で内服開始としています。
その後、頭痛の強さが0点(no pain)になることをprimary outcomeと定義しているようです。
ただし、実際は33名ほど1点(mild)なのに内服した例があったようで、これもアウトカムに含まれています。
またMBSは患者ごとに決められており、吐き気、光過敏、音過敏が挙げられています。
他、secondary outcomeは多数ありますので、結果のところで見ていこうと思います。
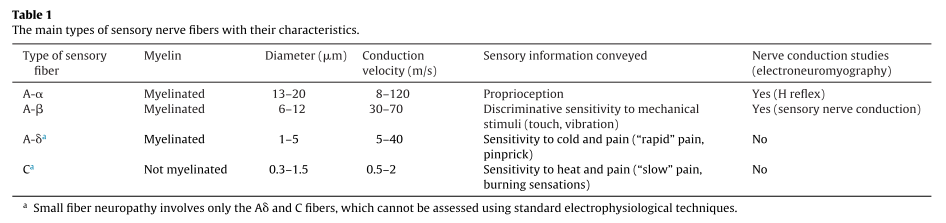
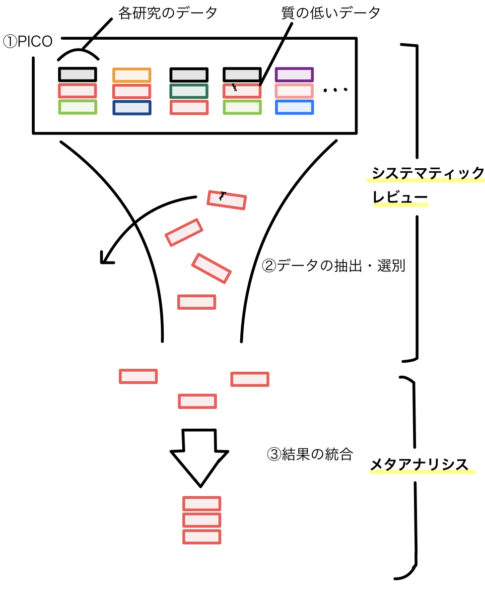
ちなみに、ここまでの患者やアウトカムの選択ですが、頭痛の臨床試験に関するガイドラインというものが発表されているようで、概ねどの試験も似通ったアウトカムとなっています。Cochraneのメタ解析でもアウトカムの選択について、こちらのガイドラインを引用していました。
Guidelines for controlled trials of drugs in migraine: Third edition. A guide for investigators
ある程度均質なアウトカムが設定されていると統合しやすいなど利点があるように思います。
統計手法
第2相試験の結果を利用して90%以上の検出力を想定し、各群570名のサンプルサイズを想定しました。
Primary outcomeは発作予防薬を共変量としたロジスティック回帰分析で行われています。発作予防薬で層別化することは先ほどの臨床試験のガイドラインでも推奨されているようで、他の試験でも通常そのようにアウトカムは評価されているようです。
また、今回の試験はプラセボvs lasmiditan 50mg,100mg,200mgということで3回仮説検定を行うことになっているため、そのまま単純に検定を行うと多重検定の問題が生じます。
多重検定の問題については以前医療統計youtubeでも紹介しました。
【解説】多重検定の問題とは | 仮説生成と仮説検証 – YouTube
そこで多重検定の問題を防ぐため、200mgのpain-freeに関するアウトカムが有意であったときに、MBS freeのアウトカムを確認し、それも有意であれば100mgのpain-freeに関するアウトカムを確認し・・・という順番で行っています。
論文中にはtesting hierarchyと記載されていますが、こうした「重要性の高い検定が有意なら次に進み、有意でなければそこで終了」という方法であれば、仮説検定全体でみたときのαエラー(family wise error rate;FWER)をα以内に保てるとされているようです。
この辺の詳細は調べていくと沼にハマりそうだったのでここまでの理解に留めておきます(汗
試験の結果
患者の振り分け(fig.1)
まずは患者の振り分けから見ていきましょう。
組み入れ基準を満たした2869例をランダム化しており、それぞれプラセボ/711名、50mg/716名、100mg/721名、150mg/721名となりました。そこから観察期間中に頭痛発作が一度もなかった62-86名をそれぞれ除外しています。
有害事象についてはSafety populationとして、この時点で抽出されている一回でも内服した群を対象に検討されています。
Primary outcomeについてはきちんとプロトコール通りに発作から4時間以内に内服し、記録をつけている群をfull analysis set populationと呼んで対象としています。
最終的な人数として
プラセボ/540名、50mg/556名、100mg/532名、150mg/528名となっています。
予定していたサンプルサイズより若干少ない程度ですね。検出力は僅かに下がると想定されますが、結果はしっかり差が出ていました。
なお、研究を中断した人は各群85-112名ほどとなっているのですが、改めて確認したら組み入れに入っていなかった(randomization failure)、フォローできなかった(lost to follow up)が多くなっています。フォローできなかった理由は詳細に記載はありませんでした。各群大きくバラつきはないですし、後述しますが結果の差も大きかったのでこの辺りの欠測は大きく問題にはならなさそうです。
ただ気になるのは僅かではあるものの、adverse eventでの中断が用量に応じて認められる点でしょうか。プラセボ、50mgでは0名、100mgで1名、200mgで4名、adverse eventによる研究中断があったようで、それなりの強度で症状が出ていたのではないでしょうか。
患者背景(table.1)
背景としては女性が8割、平均年齢は40歳代と片頭痛としては典型的な像なのかと思います。男女比1:3と言われていますので概ねこれくらいでしょう。
MIDAS scoreは平均30点台前半で、21点以上が重症 となることから、かなり重症の人が多いと言えるでしょう。頭痛専門の施設であるため、普段自分がみるような患者さんより重篤なのかもしれません。
また発作予防薬の併用は18−19%となっていました。MIDAS scoreから考えるとその都度鎮痛薬を使っていては薬剤誘発性頭痛にもなりそうなので、もっと併用されているかと思いましたが、そこまで多くはないようです。
なお、primary outcomeの一つにあがっているMBSは光過敏が最多で50%ほど、音過敏と吐き気は同じ程度で約20%ずつでした。
そして発作からの内服までの時間は概ね1時間程度であったようです。比較的現実的に可能な時間かと思います。
エンドポイント(table.2)
200mgでのPrimary outcomeについては
pain-free at 2h
200mg vs プラセボで
38.8% vs 21.3% (OR=2.3 (95%CI 1.8-3.1) P<0.001)
MBS-free
200mg vs プラセボで
48.7% vs 33.5% (OR=1.9 (95%CI 1.4-2.4) P<0.001)
となっていました。
他の用量についても同様に有意差がしっかりついています。
Secondary outcomeでは”pain-free”の維持(最初の内服後、24時間薬剤を必要としない)、痛みの改善(スケールで0まではいかない点数の低下)などもありましたが、こちらについても有意差を認めています。
有害事象
さて続いてAdverse eventsですがめまい(dizziness)が最多で
2.5%(プラセボ) vs 8.6%(50mg) vs 18.1%(100mg) vs 18.0%(200mg)
となっています。
また眠気(somnolence)がついで多く
2.0%(プラセボ) vs 5.4%(50mg) vs 4.6%(100mg) vs 6.5%(200mg)
でした。
こうした中枢神経関連の副作用は他の薬剤と比べても頻度が高く、JAMA Networkの新規薬剤とトリプタン製剤を比較したネットワークメタアナリシスの論文でも指摘されていました。
Comparison of New Pharmacologic Agents With Triptans for Treatment of Migraine: A Systematic Review and Meta-analysis
また冒頭に挙げたNEJMのレビューでもこうした副作用が運転機能にも影響するということで、lasmiditanの問題点として挙げられています。
Effects of lasmiditan on simulated driving performance: Results of two randomized, blinded, crossover studies with placebo and active controls
この論文の概説はオマケとして最後につけておきます。
こうしためまい症状が起きやすいリスク因子としてどんなものがあるかSPARTAN, SAMURAIの両試験のデータを使って事後的に検討した論文もあります。
Characterization of Dizziness After Lasmiditan Usage: Findings From the SAMURAI and SPARTAN Acute Migraine Treatment Randomized Trials
残念ながら論文の中身が読めなかったのですが、リスクとしては「lasmiditanが高用量であること」「非ヒスパニック/ラテン系」「中等度〜重度の頭痛発作」「BMIが低い」が挙げられています。
「非ヒスパニック/ラテン系」「BMIが低い」というリスク因子はガッツリ日本人に当てはまりそうで、実際第2相試験であるMONONOFUをみてみますと、被験者数がプラセボ214名、50mg 87名、100mg 208名、200mg 182名と少ないのですが、めまいの有害事象が
3.3%(プラセボ) vs 20.7%(50mg) vs 38.0% (100mg) vs 50.0% (200mg)
となっており、かなり多くなっています。日本の試験のBMIが平均22前後であるのに対し、SPARTANでは平均30前後ですので、この辺が大きく影響を及ぼしていそうです。
なお、上記のリスク因子を検討した論文によると、めまいの持続時間の中央値は1.5-2時間だったようで少なくとも長時間ではなかったようです。
他にSPARTANにおいて注目すべき点としてtableで分けて記載されているのは心疾患に関連した有害事象です。動悸や頻脈がごく少数で認められましたが1-2名ほどで用量やプラセボによる差は明らかではありませんでした。これは他の試験においても一貫して問題ないことが確認されているのでトリプタン製剤に比較した際の利点と言えるでしょう。
まとめ
さて、ラスミジタンの第3相試験であるSPARTANを読んできましたが、他の第3相試験でも同様の有効性が示され、長期の安全性試験でも問題なく、日本でも承認となりました。
片頭痛の急性期治療薬として押さえておきたい点は
- 治療効果は用量依存性にしっかり認めている
- 心血管疾患のリスク因子がある人でも使用可能
- 副作用のめまいは比較的頻度が高く(特に日本人・高用量は注意)、運転にも影響しうる
というところでしょうか。特に片頭痛の診療は運転などの活動性の高い若年者に治療薬を出すことも多いので、他の薬剤より明らかにめまい、眠気の副作用の頻度が多い点は必ず気をつけないといけないように思います。MONONOFUでの高頻度のめまいをみていると、個人的には使うとしても50mgくらいから様子見て使いたいところですね。
オマケ:lasmiditan内服後の運転機能をみた試験
上述した試験について簡単に紹介します。
Effects of lasmiditan on simulated driving performance: Results of two randomized, blinded, crossover studies with placebo and active controls
簡単にいえば薬を飲んで100km/hのスピードを想定したドライブシミュレータ(論文によれば単調な感じらしい)を1時間ほどやってもらい、どんな風になるかをみた試験のようですね。論文内では2つの試験を紹介しています。
PICOを整理しますと
○試験1
P:
21−50歳の健常者 90名
I:
ラスミジタン 50m, 100mg, 200mg
C:
プラセボもしくはアルプラゾラム 1mg(対照薬)
O:
内服後1.5時間で走行レーンのポジションがどの程度ずれるか
○試験2
P:
21−50歳の健常者 68名
I:
ラスミジタン 100mg, 200mg
C:
プラセボもしくはジフェンハイドラミン 50mg(対照薬)
O:
内服後8,12,24時間で走行レーンのポジションがどの程度ずれるか
これをそれぞれ見たものになります。なお、被験者はそれぞれの薬を盲検化された上で、間隔を3日以上空けながら全て飲むことになっています。
結果としては内服後1.5時間の試験1の場合、ラスミジタン群で用量依存性に走行時のずれが大きくなる結果となっていました。200mgがアルプラゾラム1mgに近い結果となっています。
試験2では内服後8時間ということでこのズレはかなり小さくなっておりプラセボと大きく変わらなくなっています。12、24時間ではほとんど差は目立たないように見えましたので長期に持続するような副作用ではなさそうですね。
なお、健常者を対象とした研究でもラスミジタン内服群で16-40%にめまいを認めており、この副作用というのはかなり一貫性がありそうです。やはり処方する際には必ず注意したいですね。










コメントを残す